

A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Kénsav | |||
| |||

| |||

| |||
| IUPAC-név | kénsav | ||
| Más nevek | vitriol, óleum, akkumulátorsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 7664-93-9 | ||
| ChemSpider | 1086 | ||
| EINECS-szám | 231-639-5 | ||
| KEGG | D05963 | ||
| ChEBI | 26836 | ||
| RTECS szám | WS5600000 | ||
| |||
| |||
| InChIKey | QAOWNCQODCNURD-UHFFFAOYSA-N | ||
| UNII | O40UQP6WCF | ||
| ChEMBL | 572964 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | H2SO4 | ||
| Moláris tömeg | 98,079 g/mol | ||
| Megjelenés | tiszta, színtelen, szagtalan, olajszerű viszkózus folyadék | ||
| Sűrűség | 1,84 g/cm³ (folyadék) | ||
| Olvadáspont | 10 °C | ||
| Forráspont | 337 °C (300 °C felett lassan bomlik) | ||
| Oldhatóság (vízben) | korlátlanul elegyedik exoterm reakció | ||
| Savasság (pKa) | −3, 1,99 | ||
| Viszkozitás | 26,7 cP (20 °C) | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH |
−814 kJ·mol−1[1] | ||
| Standard moláris entrópia S |
157 J·mol−1·K−1[1] | ||
| Hőkapacitás, C | 131 J/(mol·K) | ||
| Veszélyek | |||
| MSDS | ICSC 0362 | ||
| EU osztályozás | |||
| EU Index | 016-020-00-8 | ||
| NFPA 704 | |||
| R mondatok | R35 | ||
| S mondatok | (S1/2) S26 S30 S45 | ||
| Lobbanáspont | nem gyúlékony | ||
| LD50 | 2140 mg/kg (patkány, szájon át), LC50 = 25 mg/m³ (patkány, belélegezve) | ||
| Rokon vegyületek | |||
| Azonos anion | szulfátok | ||
| Rokon vegyületek | kénessav | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A kénsav (H2SO4) színtelen, nagy sűrűségű folyadék, kétértékű, erős ásványi sav. Vízzel korlátlanul elegyedik. A kénsav a kémiai ipar egyik legfontosabb vegyülete, a legnagyobb mennyiségben előállított anyag. 2001-ben 165 millió tonnát gyártottak belőle. Legnagyobb arányban a műtrágyaipar hasznosítja, de szinte minden vegyipari ágazat alapanyagként használja.
A tömény kénsav erélyes vízelvonószer. Noha előállítható a 100%-os töménységű, úgynevezett füstölgő kénsav (más néven: óleum) is, a gyakorlatban 98,3%-nál töményebb savat a kén-trioxid (SO3) párolgása miatt nem használnak. Az ólomakkumulátorok celláit 33,5%-os kénsavval töltik fel.
A kénsav előfordul a természetben is, de csak kis mennyiségben, például egyes vulkáni vidékek folyóiban, vagy a kénvegyületek oxidációjaként kén-hidrogént tartalmazó barlangokban. Az iparban a kén-trioxid kénsavban való elnyeletésével, majd az így keletkezett óleum vízzel való hígításával állítják elő.
- H2SO4 + SO3 → H2S2O7
- H2S2O7 + H2O → 2 H2SO4
Fizikai tulajdonságai
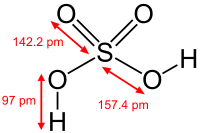
A kénsav tiszta állapotban színtelen, olajszerű, magas forráspontú (338 °C) folyadék. Ezen tulajdonságai a kénsavmolekulák között fellépő hidrogénkötésen alapulnak. A tömény vagy koncentrált kénsav 96(±2) tömegszázalékos. Magas a viszkozitása és mesterségesen állítják elő, bár kis mennyiségben a természetben is előfordulhat főleg a vulkáni tevékenység következtében. A torjai Büdös-barlang kén-hidrogént is tartalmaz és az ottani lassú oxidáció eredményezheti a kénsav megjelenését.[2]
Kémiai tulajdonságai
A tömény kénsav erős vízelvonó (higroszkópos) tulajdonságú. A levegő nedvességtartalmát megköti, a szerves anyagokat, szénhidrátokat pedig elszenesíti: a hidrogént és az oxigént elvonja belőlük, és a szén marad vissza. Még a sók kristályvizét is képes elvonni.
A kénsav a hangyasavat is elbontja, szén-monoxid fejlődése közben. Így állítanak elő a laboratóriumokban is CO-ot.
Mivel a kénsav a legerősebb savak egyike (a tömény kénsav saverősségi határt jelent az egyszerűen erős savak és a szupersavak között), a gyengébb savak viselkedhetnek vele szemben bázisként (például a salétromsav). A forró, tömény kénsav olyan erős oxidálószer, hogy oxidálja a nemfémes elemek egy részét, többek között a szenet, a ként és a foszfort.
- H2SO4 + HNO3 → HSO−4 + H2NO+3
A kénsav maró hatású anyag, ezért a vele való munka elővigyázatot igényel. A kénsav hígítását emiatt úgy végzik, hogy az üvegbot állandó kevergetése közben lassan, vékony sugárban adják a vízhez. A kénsav vízben való oldódása erősen exoterm folyamat, ezért a nem megfelelően végzett hígításkor a víz felforrhat a fejlődő hő miatt, és szétfröccsentheti a kénsavat, ami súlyos sérüléseket okozhat.
A kénsav a vízzel korlátlanul elegyedik. Vízben való oldásakor két lépésben disszociál, először hidrogén-szulfátionra, majd szulfátionra. Mint minden kétértékű sav esetén, itt is az első disszociáció megy nagyobbrészt végbe, vagyis a kénsav erősebb sav, mint a hidrogén-szulfátion. Mindkettő a kénsav savmaradékionja. A kénsav és a hidrogén-szulfátion savállandói: pKs1=-3,00; pKs2=1,99
- H2SO4 + H2O → HSO−4 + H3O+
- H2SO4 + 2 H2O → SO2−4 + 2 H3O+
- HSO−4 + H2O → SO2−4 + H3O+
A kénsav vízben való oldódásának egyenlete:
- H2SO4 + H2O = H3O+ + HSO4-
- HSO4- + H2O = H3O+ + SO42-
Egyes reakciói:
- 2 NaCl + H2SO4 = 2 HCl + Na2SO4
- Ezzel a reakcióval sósavat és glaubersót lehet előállítani.
- NaCl + H2SO4 = HCl + NaHSO4
- Ezzel a reakcióval nátrium-biszulfátot és sósavat lehet előállítani. A reakcióban a nátrium-biszulfát és a nátrium-klorid hevítése további sósavat tehet szabaddá.
- NaCl + NaHSO4 = HCl + Na2SO4
- Fe + H2SO4 = FeSO4 + H2
Szulfátok
A hidrogén-szulfátok és a szulfátok a kénsav sói. A hidrogén-szulfátok vízzel hidrolizálnak, átadják a protonjukat, ezért ezeknek vizes oldata savas kémhatású.
- Na+ (aq) + HSO−4 (aq) → Na+ + SO2−4 + H3O+
Vagyis az oldatban az oxóniumionok kerülnek túlsúlyba a hidroxidionokkal szemben.
Az alumínium-szulfát, az alumínium-kálium-szulfát, az ammónium-szulfát, a réz-szulfát és a vas(III)-szulfát vizes oldata is savas kémhatású.
A híg kénsav reakcióba lép a vassal, a magnéziummal, és az alumíniummal. Nem reagál a rézzel és az ólommal. Vassal való reakciójának egyenlete:
- Fe + H2SO4 = H2 + FeSO4 vas-szulfát
A forró tömény kénsav a rezet is feloldja, két lépésben, mivel előbb oxidálja:
- Cu + cc. H2SO4 → CuO + H2O + SO2
- CuO + H2SO4 → CuSO4 + H2O
Hasonlóan viszi oldatba a forró tömény kénsav a higanyt és az ezüstöt is.
A tömény kénsav oxidálja a vasat, tömör vas-oxid réteg alakul ki. Ezért lehet a kénsavat vastartályban szállítani.
Az ólmot már a híg kénsav is passziválja, az ólom felületén oldhatatlan ólom-szulfát keletkezik.
A tömény kénsav lúgokkal, például nátrium-hidroxid oldattal közömbösíthető. Ekkor nátrium-szulfát (glaubersó) és víz keletkezik.
- H2SO4 + 2 NaOH → Na2SO4 + 2 H2O
- H2SO4 + Ca(OH)2 → CaSO4 + 2 H2O
Kénsavészterek
A kénsavészterek a kénsav és különböző alkoholok vegyületei. Nagy gyakorlati jelentőségük van, mosószerként használatosak. Előnyük a szappanokkal szemben, hogy kemény vízben vagy savas közegben is kifejtik hatásukat. Gyártásuk során a kénsavnak csak egyik felét észteresítik el, a másik savas csoportot sóvá alakítják.
Kénsavgyártás
A kénsavgyártás alapanyaga többnyire elemi kén, illetve a fém-szulfidok. A ként elégetve vagy a szulfidokat pörkölve kén-dioxid keletkezik.
- S + O2 → SO2
- 2 ZnS + 3 O2 → 2 ZnO + 2 SO2
- HgS + O2 → Hg + SO2
A kén-dioxidot tovább oxidálják, ilyenkor kén-trioxid keletkezik:
- 2 SO2 + O2 ⇌ 2 SO3
Az exoterm reakció egyensúlyra vezet, ezért célszerű alacsony hőmérsékleten (400-500 °C) végezni, azonban homogén fázisban a reakció sebessége nagyon kicsi. A reakciósebességet vanádium-pentoxid katalizátor alkalmazásával növelik. A kén-trioxidot gyakorlati okok miatt nem vízben, hanem tömény kénsavban nyeletik el, majd az így keletkező dikénsavat (pirokénsav, óleum) vízben a megfelelő töménységűre hígítják.
Felhasználása
A kénsav vegyipari alapanyag, emellett a laboratóriumban is gyakran használják. A kénsavat műtrágyagyártásra, mosószergyártásra, festékgyártásra, gyógyszergyártásra és robbanószerek gyártására is használják. Emellett kénsav az ólomakkumulátorok töltőfolyadéka.
Jegyzetek
- ↑ a b Zumdahl, Steven S.. Chemical Principles 6th Ed.. Houghton Mifflin Company, A23. o. (2009). ISBN 0-618-94690-X
- ↑ Kén oxidjai és oxosavai (magyar nyelven). ttko.hu. (Hozzáférés: 2023. augusztus 9.)
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.
Analóg multiméterek túlterhelés elleni védelme
Egyenáram
Egyenáram mérése
Egyenirányítós lengőtekercses műszer
Elektromágnes (fizika)
Elektromos feszültség
Elektromos térerősség
Fáziseltolódás
Fázismutató
Fajlagos ellenállás
Feszültséggenerátor
Feszültségváltó
Forgó mágneses tér
Háromfázisú hálózat
Hőelektromosság
Hatásos ellenállás
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.
