

A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Kálium-hidroxid | |

| |
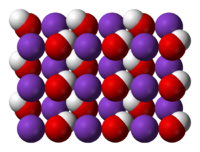
| |
| IUPAC-név | kálium-hidroxid |
| Más nevek | marókáli |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 1310-58-3 |
| EINECS-szám | 215-181-3 |
| RTECS szám | TT2100000 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | KOH |
| Moláris tömeg | 56,11 g/mol |
| Megjelenés | higroszkópos, fehér rögök |
| Halmazállapot | szilárd |
| Sűrűség | 2,04 g/cm³ (20 °C) |
| Olvadáspont | 360-380 °C |
| Forráspont | 1379 °C |
| Oldhatóság (vízben) | 1130 g/l (20 °C) |
| Kristályszerkezet | |
| Kristályszerkezet | monoklin[1] |
| Veszélyek | |
| EU osztályozás | maró hatású (C) |
| EU Index | 019-002-00-8 |
| R mondatok | R22, R35 |
| S mondatok | (S1/2), S26, S36/37/39, S45 |
| Lobbanáspont | nem gyúlékony |
| Rokon vegyületek | |
| Azonos kation | a kálium vegyületei |
| Azonos anion | hidroxidok |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A kálium-hidroxid vagy marókáli egy szervetlen vegyület, amelynek képlete KOH. Színtelen kristályokat alkot, erősen higroszkópos. Erős bázis. Vizes oldatát a kereskedelemben, háztartási tisztítószerként, hideg zsíroldó néven forgalmazzák.[2]
Története
Jellemzői
A kálium-hidroxid szobahőmérsékleten szilárd halmazállapotú, erősen nedvszívó (higroszkópos) kristályos anyag. Levegőn gyorsan elfolyósodik, és a levegő szén-dioxid-tartalmával reagálva kálium-karbonáttá alakul. Vízben és alkoholban jól oldódó, a nátrium-hidroxidnál erősebb bázis, vizes oldata a kálilúg. Vizes oldatban teljesen disszociál, oldata erősen maró, lúgos kémhatású. Olvadt állapotban a szilikátokat, így az üveget is feloldja.
- Kálium-hidroxid és szén-dioxid reakciója kálium-karbonát és víz keletkezése közben.
Előfordulása, előállítása
Előállítható kálium-klorid oldat elektrolízisével vagy kálium-karbonát és kalcium-hidroxid reakciója révén. Vizes oldatban végezve az utóbbi kísérletet a vízben oldhatatlan kalcium-karbonát kicsapódik, és kiszűrhető az oldatból.
- Kálium-karbonát és kalcium-hidroxid reakciója kálium-hidroxid és kalcium-karbonát keletkezése közben.
Felhasználása
Felhasználják a laboratóriumokban vegyszerként, lúgos akkumulátorokban elektrolitként, valamint káliszappan és más káliumvegyületek előállítására.
- A VIII. Magyar Gyógyszerkönyvben Kalii hydroxidum néven hivatalos.
- Az élelmiszeriparban széles körben alkalmazzák, például a gyümölcsök héjának kémiai úton történő eltávolítására, csokoládé és kakaó készítése során, karamellel történő színezésnél, olajbogyó tartósításánál, valamint egyes pékárukban is előfordulhat, valamint az annatto (E160b) használata estén is. Élelmiszer-adalékanyagként, E525 néven alkalmazzák. Napi maximum beviteli mennyisége nincs meghatározva, valamint élelmiszerek esetén nincs ismert mellékhatása, mert rendkívül erős lúgossága miatt csak nagyon kis mennyiségben alkalmazható.[3]
- Az olcsóbb háztartási hipó mellett ez a legfontosabb konyhai tisztítószer. Főleg a konyhai sütők zsírmentesítésére, a megszenesedett ételmaradványok eltávolítására szokták használni.
Élettani tulajdonságok
Az anyag maró hatású a bőrre, a szemre és lenyelve. Maradandó égési sérüléseket okoz!
Óvintézkedések
Nagyon fontos a megfelelő védőeszköz. Gumikesztyű, védőszemüveg vagy arcvédő légzésvédelemmel kombinálva. A levegő nedvességtartalmával érintkezve elpattanhatnak a kristályok, így akár a szembe is kerülhetnek.
Források
- ↑ James A. Ibers, Junji Kumamoto, and Robert G. Snyder (1960). „Structure of Potassium Hydroxide: An X-Ray and Infrared Study”. J. Chem. Phys. 33 (4), 1164-1170. o. DOI:10.1063/1.1731351.
- ↑ A hideg zsíroldó alapvetően kálium-hidroxid vizes oldata, de a gyártók, kisebb arányban, adalékanyagokat is tehetnek a termékbe, például, 2-aminoetanolt és 2-butoxietanolt.
- ↑ Food-Info.net : E-numbers : E525 : Potassium hydroxide
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.
Analóg multiméterek túlterhelés elleni védelme
Egyenáram
Egyenáram mérése
Egyenirányítós lengőtekercses műszer
Elektromágnes (fizika)
Elektromos feszültség
Elektromos térerősség
Fáziseltolódás
Fázismutató
Fajlagos ellenállás
Feszültséggenerátor
Feszültségváltó
Forgó mágneses tér
Háromfázisú hálózat
Hőelektromosság
Hatásos ellenállás
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.

