

A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| AlumÃnium-klorid | |
 AlumÃnium-klorid hexahidrÃĄt | |
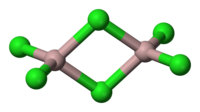 AlumÃnium-triklorid dimer | |
| IUPAC-nÃĐv | AlumÃnium-triklorid |
| KÃĐmiai azonosÃtÃģk | |
|---|---|
| CAS-szÃĄm | (vÃzmentes) (hexahidrÃĄt) |
| PubChem | 24012 |
| ATC kÃģd | D10AX01 |
| GyÃģgyszer szabadnÃĐv | aluminium chloride |
| GyÃģgyszerkÃķnyvi nÃĐv | Aluminii chloridum hexahydricum |
| KÃĐmiai ÃĐs fizikai tulajdonsÃĄgok | |
| KÃĐmiai kÃĐplet | AlCl3 |
| MolÃĄris tÃķmeg | 133,34 g/mol (vÃzmentes) 241,432 g/mol (hexahidrÃĄt) |
| MegjelenÃĐs | FehÃĐr vagy sÃĄrga szÃnÅą, szilÃĄrd |
| SÅąrÅąsÃĐg | 2,44 g/cmÂģ[1] |
| OlvadÃĄspont | 180 °C-on szublimÃĄl, 262 °C-on bomlik[1] |
| OldhatÃģsÃĄg (vÃzben) | 43,9 g/100 ml (0 °C) 44,9 g/100 ml (10 °C) 45,8 g/100 ml (20 °C) 46,6 g/100 ml (30 °C) 47,3 g/100 ml (40 °C) 48,1 g/100 ml (60 °C) 48,6 g/100 ml (80 °C) 49 g/100 ml (100 °C) |
| VeszÃĐlyek | |
| EU osztÃĄlyozÃĄs | MarÃģ (C)[2] |
| R mondatok | R34[2] |
| S mondatok | (S1/2), S7/8, S28, S45[2] |
| LD50 | 3450 mg/kg (patkÃĄny, szÃĄjon ÃĄt)[1] |
| Rokon vegyÞletek | |
| Azonos kation | AlumÃnium-fluorid AlumÃnium-bromid AlumÃnium-jodid |
| Azonos anion | BÃģr-triklorid Gallium(III)-klorid Indium(III)-klorid Tallium(III)-klorid MagnÃĐzium-klorid |
| Rokon Lewis-savak | Vas(III)-klorid BÃģr-trifluorid |
| Ha mÃĄskÃĐnt nem jelÃķljÞk, az adatok az anyag standardÃĄllapotÃĄra (100 kPa) ÃĐs 25 °C-os hÅmÃĐrsÃĐkletre vonatkoznak. | |
Az alumÃnium-klorid az alumÃnium klÃģrral alkotott vegyÞlete, kloridja. KÃĐplete AlCl3. FehÃĐr szÃnÅą kristÃĄlyokat alkot. MÃĄr alacsonyabb hÅmÃĐrsÃĐkleten is pÃĄrolog. 180 °C-on szublimÃĄl, ezÃĐrt csak nagyobb nyomÃĄson lehet megolvasztani. ErÅsen higroszkÃģpos, magÃĄba szÃvja a levegÅ nedvessÃĐgÃĐt ÃĐs sÅąrÅą folyadÃĐkkÃĄ alakul. JÃģl oldÃģdik vÃzben. Szerves oldÃģszerek (pÃĐldÃĄul alkohol, ÃĐter, aceton) is jÃģl oldjÃĄk. Vizes oldatÃĄbÃģl a hexahidrÃĄtja (AlCl3 · 6 H2O) kristÃĄlyosÃthatÃģ ki.
Szerkezete
Az alumÃnium-klorid monomer AlCl3 molekulÃĄi elektronhiÃĄnyosak, ezÃĐrt instabilak. Ezek a molekulÃĄk kÃķnnyen dimerizÃĄlÃģdnak, ekkor Al2Cl6 dimer molekulÃĄk keletkeznek. Az alumÃnium-klorid gÅzei kÃķrÞlbelÞl 700 °C hÅmÃĐrsÃĐkletig tartalmaznak ilyen molekulÃĄkat, magasabb hÅmÃĐrsÃĐkleten a molekulÃĄk disszociÃĄlnak. Ezek a molekulÃĄk kÃĐt AlCl4 tetraÃĐderbÅl ÃĐpÞlnek fel, a kÃĐt tetraÃĐder egyik ÃĐle kÃķzÃķs. Ha a molekulÃĄk kristÃĄlyrÃĄcsba rendezÅdnek, deformÃĄlÃģdnak. A szilÃĄrd alumÃnium-klorid kristÃĄlyt lazÃĄn ÃķsszekapcsolÃģdÃģ AlCl6 oktaÃĐderek ÃĐpÃtik fel.

KÃĐmiai tulajdonsÃĄgai
A vegyÞlet vÃz hatÃĄsÃĄra hidrolizÃĄl, vizes oldata savas kÃĐmhatÃĄsÚ.
A kÃĐpzÅdÅ alumÃnium-hidroxid vÃzben rosszul oldÃģdik, csapadÃĐkkÃĐnt vÃĄlik ki. Emiatt az oldat zavaros lesz. A tÃķmÃĐnyebb oldat a fejlÅdÅ hidrogÃĐn-klorid miatt fÞstÃķlÃķg. AddÃciÃģs vegyÞleteket kÃĐpez ammÃģniÃĄval, kÃĐn-dioxiddal ÃĐs sok szerves vegyÞlettel.
ElÅÃĄllÃtÃĄsa
VÃzmentes alumÃnium-kloridot Úgy ÃĄllÃtanak elÅ, hogy alumÃniumreszelÃĐket reagÃĄltatnak klÃģrral. A reakciÃģ nyersanyaga drÃĄga, ezÃĐrt leginkÃĄbb timfÃķldbÃģl ÃĄllÃtjÃĄk elÅ szÃĐn-monoxid ÃĐs klÃģrgÃĄz, illetve az ezekbÅl kÃĐpzÅdÅ foszgÃĐn segÃtsÃĐgÃĐvel.
TimfÃķld helyett bauxit is hasznÃĄlhatÃģ, de a bauxitbÃģl elÅÃĄllÃtott alumÃnium-klorid gyakran vasat tartalmaz. A vegyÞlet vizes oldatÃĄt alumÃnium-hidroxidbÃģl ÃĄllÃtjÃĄk elÅ sÃģsavval.
FelhasznÃĄlÃĄsa
Szerves kÃĐmiai szintÃĐzisekben a FriedelâCrafts-reakciÃģk katalizÃĄtora. KatalizÃĄtorkÃĐnt alkalmazzÃĄk mÅągyantÃĄk, mÅąanyagok, gumi ÃĐs kenÅanyagok gyÃĄrtÃĄsakor. Sok kondenzÃĄciÃģs reakciÃģt gyorsÃt. IzzadÃĄs elleni szereket is kÃĐszÃtenek belÅle.
ForrÃĄsok
- Erdey-GrÚz Tibor: Vegyszerismeret
- Nyilasi JÃĄnos: Szervetlen kÃĐmia
HivatkozÃĄsok
- â a b c Az alumÃnium-klorid biztonsÃĄgi adatlapja (Merck) (nÃĐmetÞl)
- â a b c Az alumÃnium-klorid veszÃĐlyei (ESIS)[halott link]
A lap szÃķvege Creative Commons Nevezd meg! â Ãgy add tovÃĄbb! 3.0 licenc alatt van; egyes esetekben mÃĄs mÃģdon is felhasznÃĄlhatÃģ. RÃĐszletekÃĐrt lÃĄsd a felhasznÃĄlÃĄsi feltÃĐteleket.
ïŧŋAnalÃģg multimÃĐterek tÚlterhelÃĐs elleni vÃĐdelme
ïŧŋEgyenÃĄram
ïŧŋEgyenÃĄram mÃĐrÃĐse
ïŧŋEgyenirÃĄnyÃtÃģs lengÅtekercses mÅąszer
ïŧŋElektromÃĄgnes (fizika)
ïŧŋElektromos feszÞltsÃĐg
ïŧŋElektromos tÃĐrerÅssÃĐg
ïŧŋFÃĄziseltolÃģdÃĄs
ïŧŋFÃĄzismutatÃģ
ïŧŋFajlagos ellenÃĄllÃĄs
ïŧŋFeszÞltsÃĐggenerÃĄtor
ïŧŋFeszÞltsÃĐgvÃĄltÃģ
ïŧŋForgÃģ mÃĄgneses tÃĐr
ïŧŋHÃĄromfÃĄzisÚ hÃĄlÃģzat
ïŧŋHÅelektromossÃĄg
ïŧŋHatÃĄsos ellenÃĄllÃĄs
ïŧŋImpedancia
ïŧŋIndukciÃģs mÅąszer
ïŧŋKÃķrmÃĄtrix
ïŧŋKÃķzÃķs mÃģdusÚ elnyomÃĄs
ïŧŋKalciumfÃĐny
ïŧŋKif hÃĄlÃģzat
ïŧŋLÃĄgyvas
ïŧŋLÃĄtszÃģlagos ellenÃĄllÃĄs
ïŧŋLineÃĄris ÞzemÅą tÃĄpegysÃĐg
ïŧŋMÅąveleti erÅsÃtÅ
ïŧŋManganin
ïŧŋMeddÅ ellenÃĄllÃĄs
ïŧŋMeddÅ teljesÃtmÃĐny mÃĐrÃĐse
ïŧŋMillman-tÃĐtel
ïŧŋNorton-tÃĐtel
ïŧŋPiezoelektromossÃĄg
ïŧŋPiroelektromossÃĄg
ïŧŋPotenciomÃĐter
ïŧŋReplusz
ïŧŋRezgÅkÃķr
ïŧŋSeebeck-effektus
ïŧŋSzuperpozÃciÃģ (elektronika)
ïŧŋThÃĐvenin-tÃĐtel
ïŧŋVÃĄltakozÃģ ÃĄram
ïŧŋVÃĄltakozÃģ ÃĄram mÃĐrÃĐse
ïŧŋVillamossÃĄgtan
ïŧŋVillamos fogyasztÃĄsmÃĐrÅ
ïŧŋWien-hidas oszcillÃĄtor
ïŧŋZener-effektus
A lap szÃķvege Creative Commons Nevezd meg! â Ãgy add tovÃĄbb! 3.0 licenc alatt van; egyes esetekben mÃĄs mÃģdon is felhasznÃĄlhatÃģ. RÃĐszletekÃĐrt lÃĄsd a felhasznÃĄlÃĄsi feltÃĐteleket.


