

A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Oxálsav | |||
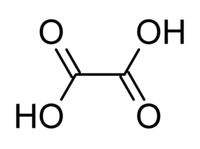 Oxálsav | |||
 Oxálsav pálcikamodellje |
 Oxálsav kalottamodellje | ||
| IUPAC-név | oxálsav | ||
| Szabályos név | etándisav | ||
| Más nevek | Sóskasav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 144-62-7 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | H2C2O4 (vízmentes) H2C2O4·2H2O (dihidrát) | ||
| Moláris tömeg | 90,04 g/mol | ||
| Megjelenés | fehér kristályok | ||
| Sűrűség | 1,90 g/cm³ (vízmentes, 17 °C)[1] 1,635 g/cm³ (dihidrát, 18,5 °C)[1] | ||
| Olvadáspont | 157 °C felett bomlik[1] | ||
| Oldhatóság (vízben) | 90-100 g/l (20 °C)[1] | ||
| Savasság (pKa) | pKs1 = 1,37 pKs2 = 3,81[2] | ||
| Veszélyek | |||
| EU osztályozás | Ártalmas (Xn)[3] | ||
| NFPA 704 | |||
| R mondatok | R21/22[3] | ||
| S mondatok | (S2), S24/25[3] | ||
| Lobbanáspont | 166 °C | ||
| LD50 | 7500 mg/kg (patkány, szájon át)[1] | ||
| Rokon vegyületek | |||
| Rokon vegyületek | oxalil-klorid dinátrium-oxalát kalcium-oxalát difenil-oxalát | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Oxálsav, más néven: sóskasav, etándisav. Két bázisú (azaz besorolása: dikarbonsav), széntartalmú organikus sav. A legegyszerűbb kétértékű karbonsav. Kémiai képlete: HOOC–COOH. Sói és észterei az oxalátok.
Az oxálsav szó a görög okszálisz (ὀξαλίς = erdei sóska) szóból származik, latin közvetítéssel (oxalis).[4]
Története
François Pierre Savary (Fribourg, Svájc) fedezte fel 1773-ban.
Az oxálsav volt az első szerves anyag, amit szervetlen anyagokból állítottak elő ezzel bizonyítva, hogy az élő szervezetre a szervetlen környezet is biokémiailag hatással van.
A XIX. század második felétől elkezdődött a szerves és szervetlen kémia ötvözése. Megindult a szerves molekulák szervetlen anyagokból történő szintetizálása, amely a gyógyszeripar egyik alappillére lett a XXI. századra.
Tulajdonságai
Fehér kristályos vegyület.
Az oxálsav egyhajlású prizmákban kristályosodik, amelyek két molekula kristályvizet tartalmaznak (H2C2O4·2 H2O). Vízben és alkoholban könnyen oldódik (2 sr. kristályos oxálsav szobahőmérsékleten 9 sr. vízben feloldódik), oldata erősen savanyú ízű és savas kémhatású. Oxidáló anyagok (kálium-permanganát) igen könnyen szén-dioxiddá és vízzé oxidálják, ezért az oxálsav erélyes redukálószer. Az iparban a karton-, selyem- és gyapotfestészetben, a kémiai laboratóriumokban pedig normál (szabályos) oldatok készítésére és a különféle oxálsavsók előállítására használják. Nagyobb adagban a szervezetre mérgező hatású. Az oxálsav legegyszerűbben mészvízzel ismerhető fel, amellyel fehér, ecetsavban oldhatatlan csapadékot ad. Mennyiségi meghatározása leginkább kálium-permanganát oldattal történik titrálás útján. Analitikai kémiában az egyik legelterjedtebb titeralapanyag, mivel 99,9 %-os tisztaság is elérhető. Általában lúgok mennyiségi meghatározására használják.
Előfordulása
Előfordul a sóskában, spenótban és számos más növényben (az Oxalis és a Rumex fajokban), azonkívül az állati szervezetben (a vizeletben) részint szabad állapotban, részint különféle sók alakjában. Kalciumsója a vesekő leggyakoribb alkotója. A természetben található humboltin nevű ásvány nem egyéb, mint vas(II)-oxalát, a whewellit pedig kalcium-oxalát. Oxálsav képződik igen sok széntartalmú vegyület oxidációjakor, így a cukorféleségeknek, a szénhidrátoknak, stb. salétromsavval való oxidálásakor.
Kalciumsója vízben oldhatatlan (ezért okozhat vesekövet). Savanyú kálium sója (HOOC-COOK) a rozsdafoltot eltávolítja.
Reakcióképessége, reakciói
Az oxálsav kétbázisú sav lévén, számos sót alkot, amelyeket oxalátoknak neveznek. Ezek közül fontosabbak:
- Kálium-oxalát (K2C2O4.H2O), amely az oxálsav és a kálium-karbonát telítése, és az oldatnak kikristályosítása útján készül. Vízben könnyen oldódik. Ezt a sót a barnakő (MnO2) meghatározására és a fényképészetben használták. Oxálsavval elegyítve savanyú sóvá, kálium-hidrooxaláttá (KHC2O4.H2O) alakul, mely a természetben számos savanyú ízű növény (például sóska) nedvében megtalálható és legegyszerűbben úgy készül, hogy az oxálsav felét kálium-karbonáttal telítik és a másik felét hozzáöntve kikristályosítják.
- Kálium-quadrioxalát , amely fő alkatrészét képezi a kereskedésben található ún. sóskasónak és amit a háztartásban tinta- és rozsdafoltok eltávolítására használnak. A kálium-oxalátokhoz teljesen hasonlók a megfelelő nátrium- és ammóniumsók.
- Kalcium-oxalát (CaC2O4.H2O), fehér, por alakú csapadék alakjában válik le, ha a vízben oldható oxalátokhoz kalcium-klorid oldatot öntünk. Megtalálható a növényi és az állati szervezetben (vizeletben), a húgykövekben stb. Vízben és ecetsavban oldhatatlan, de sósavban v. salétromsavban igen könnyen feloldódik. Erősebb hevítéskor kalcium-karbonátra és széndioxidra bomlik. A súly szerinti elemzésben rendszerint e só alakjában választják le a kalciumot. A kalcium-oxaláthoz teljesen hasonló a bárium- és stroncium-oxalát.
- Ferrooxalát (FeC2O4.2H3O), citromsárga csapadék, mely ferroszulfát- és kálium-oxalát oldatok elegyítésekor képződik. A ferrooxalátnak a kálium-oxaláttal való kettős sóját kiváló redukáló hatásánál fogva a fotográfiában mint igen jó «előhívót» használják.
- Ferrioxalát , frissen készült ferrihidroxidnak oxálsavban való oldása útján kapható. A fény a ferrioxalátot ferrooxaláttá redukálja, ezért az előállításnak sötétben kell történni. Hasonló összetételűek a kromo- és kromioxalátok, amelyek igen szép színűek. Az oxálsavban a hidrogénatomok különféle alkoholgyökökkel (metil, etil stb.) helyettesíthetők és ekkor az oxálsavnak különféle összetett éterei keletkeznek, amelyek azonban csak tudományos érdekűek. Hasonlóképp nem bírnak gyakorlati fontossággal az oxálsav különféle amidjai és más bonyolultabb összetételű vegyületei.
Előállítása
Nagyban való előállítása úgy történik, hogy fűrészport kálium- és nátrium-hidroxid elegyével összekeverve, vas üstökben 200-220 °C-ra hevítenek, ekkor nátrium- és kálium-oxalát képződik. A megolvadt barna tömeget vízzel kivonják, és oltott mésszel főzik; ekkor kalcium-oxalát válik ki, amelyet kénsavval bontanak el, és a megszűrt oldatból kikristályosítják. Kicsiben legcélszerűbben úgy készíthető, hogy 1 rész cukrot 5 rész salétromsavval (fs. 1,245) főzünk, és a folyadékot kikristályosítjuk. A kereskedelemben előforduló oxálsav rendszerint nem tiszta, de igen könnyen megtisztítható úgy, hogy vízben oldjuk, és az oldatot besűrítés után lassan kihűlni hagyjuk.
Jegyzetek
- ↑ a b c d e Az oxálsav vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2010. 12. 28. (JavaScript szükséges) (angolul)
- ↑ Négyjegyű függvénytáblázatok, összefüggések és adatok. Nemzeti tankönyvkiadó, 2006.
- ↑ a b c Az oxálsav (ESIS)[halott link] (németül)
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 108. o. ISBN 963 8334 96 7
Források
| Ez a szócikk részben vagy egészben a Pallas nagy lexikonából való, ezért szövege és/vagy tartalma elavult lehet.
Segíts nekünk korszerű szócikké alakításában, majd távolítsd el ezt a sablont! |
További információk
|
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.
Émile Faguet
Émile Louis Victor de Laveleye
Émile Ollivier
Épületszárny
Ívhíd
Újplatonizmus
Abel-François Villemain
Adományrendszer
Albert Sorel
Albert Venn Dicey
Arcueil
Areioszpagosz
Argirodit
Asztaltáncoltatás
Augusto Pierantoni
August Fournier
Azovegyület
A közgazdaságtan története
Basszus
Benjamin Disraeli
Benzol
Benzolszármazékok
Berlini szerződés
Bezerédj család
Bizalmam az ősi erényben
Bodrog vármegye
Bolondvár
Camillo Benso di Cavour
Carl August von Steinheil
Charles-Bonaventure de Longueval
Church of England
Cista
Citromsav
Clam család
Csésze (edény)
Dénár
Denudáció
Dextrin
Diorit
Dudvág
Ecloga legum
Egyetemes postatörténet
Emilio Castelar
Enrico Cialdini
Episzkopalizmus
Eposz
Erkély
Ernst Curtius
Erzsébet Filippina Mária francia királyi hercegnő
Eskü
Esperes
Exemptio
Fáy család
Fémlemez
Földárja
Fővárosi Közmunkák Tanácsa
Fűrész
Fabius Planciades Fulgentius
Fedélzet
Fejérvármegyei és Székesfejérvár városi történelmi s régészeti egylet
Felségsértés
Filantropizmus
Fokozatos felelősség
Fok (földrajz)
František Ladislav Rieger
Franz Anton von Kolowrat-Liebsteinsky
Franz Michael Felder
Georgikon
Giovanni Battista Donati
Giuseppe Garibaldi
Hámor (fémfeldolgozás)
Hajóhíd
Hajótörés
Hanglyuk
Herulok
Hjalmar Hjorth Boyesen
Holland irodalom
Hordó (tartály)
Horváth-Stansics család
Hugh Latimer
I. Abdul-Medzsid oszmán szultán
II. Mahmud oszmán szultán
II. Róbert skót király
Internátus
Iskola
Istálló
Jacopo Sansovino
Jakob Böhme
Jean-Barthélemy Hauréau
Jean de La Fontaine
Jeszenik-hegység
Johann Bernhard Basedow
Johann Julius Hecker
John Ross Browne
Károlyi István (politikus, 1797–1881)
Közhasznú Esmeretek Tára
Kübelé
Kafferek
Kalapács (szerszám)
Kalcinálás
Kankalinfélék
Karl Friedrich Lessing
Karl Friedrich von Steinmetz
Kefe
Kerékvető
Királysértés
Kitt (kötőanyag)
Kiváltság
Konjunktúra
Konkréció
Koronaőrök
Léonce Guilhaud de Lavergne
Léon Gambetta
Létra
Lajos-csatorna
Latorca
Legyező
Lengyel irodalom
Levélállás
Lex
Libráció
Likőr
Márvány
Méhrepedés
Magyar Állam (napilap)
Magyar időszaki lapok a 19. században
Magyar Orvosi Könyvkiadó Társulat
Manysik
MATE Georgikon Campus
Mauretania
Melegágy
Mikrolit (ásvány)
Minoriták
Muhammad Ali egyiptomi alkirály
Nádori testőrség
Népszokások
Nafta
Norvég irodalom
Numa Denis Fustel de Coulanges
Országos Nőképző Egyesület
Oszloprend
Oxálsav
Paragenezis
Pergamon
Pierre Puget
Polgári házasság a dualizmus korában
Polgári halál
Portugál irodalom
Pozsonyi gróf
Praetorianusok
Rózsa rend (Brazília)
Rózsa rend (Honduras)
Robert Southey
Rodolfo Lanciani
Rohan család
Sátor
Sürgöny (diplomácia)
Saint-simonizmus
Sedan (Franciaország)
Skót irodalom
Skandinavizmus
Sorompó
Special:CentralAutoLogin/start?type=1x1
Stephan von Jovanović
Széchy család (felsőlendvai)
Szénaszárító
Szörny
Szőnyi béke
Szalol
Szarkofág
Szarv
Szerb irodalom
Takarmány
Tarack (löveg)
Telekkönyv
Temető
Tengernagy
Toldalagi család
Trágya
Trákia
Válság (gazdaság)
Váza
Vetésforgó
Viaszos vászon
Vittorio Alfieri (drámaíró)
Zárnélküli pörgekarúak
Zárosperemű pörgekarúak
Zátony
Zuávok
A lap szövege Creative Commons Nevezd meg! – Így add tovább! 3.0 licenc alatt van; egyes esetekben más módon is felhasználható. Részletekért lásd a felhasználási feltételeket.
